Nn指示薬 キレート滴定の指示薬(錯形成→ 赤:遊離→ 青) edta溶液 滴定剤 有機廃液タンクへ (注ぎ口にろ紙をつけておくこと!) 実験の注意事項 edta滴下 (1) 『ホールピペットで取る』と指定が無いものは大体でok!金属イオンの滴定法をキレート滴定法と呼ぶのもそのた めです 3 滴定試薬としての応用(キ レート滴定法) 3・1 キレート滴定法の原理 ふたたび反応式(iii)に ついて考えてみましょう あ る金属イオン(m)の 水溶液にedta溶 液(y)を 滴 キレート滴定で脱イオン水を使う理由を教えてください。 カチオンがあると、滴定に影響するから。 解決済み 質問日時: 21/5/10 1503 回答数: 1 閲覧数: 3 教養と学問、サイエンス > サイエンス > 化学 化学のキレート滴定についての計算です。
Syllabus Kosen K Go Jp
キレート滴定 考察 知恵袋
キレート滴定 考察 知恵袋-キレート滴定では、金属イオンとキレート試薬(もっぱらedtaが使われる)が安定な錯体を作ることを利用する。 したがって、たとえば ebt の場合は滴定の終点として、完全に赤みの消えたところを取る。 キレート滴定では、ph の設定に注意を払う必要がとなる。 キレート滴定では、この至適 pH を保つために緩衝液が用いられる! XIII13 補助錯化剤 一般にキレート滴定はかなり高い pH で行なうが、このとき金属水酸化物を沈殿させな いように、 EDTA より Kf の小さい錯化剤(=補助錯化剤 )を共存させることが




シラバス Manualzz
滴定用キレート試薬として、ドータイト2na(edta2ナトリウム 塩)、その他ドータイト金属指示薬、キレート滴定用補助試薬など、 キレート滴定に必要な試薬類は全部とりそろえているので、ご利 用いただきたい。 nc h2ch2 n ch 2cooh hoocch2 ch2cooh hooc 2 on o n m ch2 ch29 どのように読みましたか。 ×26 cm3 262 263 264 1目盛=01 cm3 として読むと、 (ケースA) 2 cm3 3 cm3 「キレート滴定は、これまでに何度も繰り返し行ってきたので、 スムーズに実験を進めることができました。 そして、満足のいく結果も出せたので、とても楽しく実験ができました! これからも基礎的な実験の技術を大切にしながら、
水の硬度測定 1 はじめに 硬度 1) とは,水に含まれるCa 2 とMg 2 の量を表す指標であり,この値に基づいて軟水や硬水 2) といった水の硬さが決められている。 軟水は口当たりがまろやか,硬水は苦みのような口当たりといわれている。近年,スーパーなどで多くの種類のミネラルウォーターをキレート生成反応: キレート滴定(chelatometric titration),陽イオンの定量。 沈澱反応: 沈澱滴定(precipitation titration),陰イオンの定量。 酸化還元反応: 酸化還元滴定(oxidation reduction titration) 滴定の操作は次のパータンである:Fe2+:phen=1:3の金属キレートを生成する反応を利用している。 この金属錯体は長時間変化せず安定で、1,10 -フェナントロリンと錯体を形成するのは 2価の鉄のみである。鉄は水溶液中で3価で存在することがあるので、還元剤として、
EDTA と金属キレートのK f 値→p18, 表12 <例:EDTA とMg2> K f = 49×108 log K f = 8 log 49 = 869 ML n M Ln 8 キレート滴定 多座配位子EDTA(標準液)が 金属イオン(Zn 2, Mg 2, Ca , Al3, Cu 等)と 水溶液中で安定な可溶性のキレート化合物を生成する ことを利用した洋白中のニッケルの分離と定量 ニッケルはジメチルグリオキシム溶液を加えてニッケル塩 ni(c 4 h 7 n 2 o 2) 2 を沈殿分離した後、キレート滴定で定量します。 ここでジメチルグリオキシムでニッケルを沈殿させる前に、ジメチルグリオキシムが銅と錯体を作って浪費されるのを防ぐため、銅をパックテストとキレート滴定の結果を総合して 考察すると、数値的には入善町の水は「おいしい 水」の条件に適しているとわかる。混ざりものが少 なくきれいであることで、そのまま生活用水とし て利用できる。入善町の水がきれいでおいしいと




Microsoft Word 目次注意事項2 Doc



至急お願いします キレート滴定の実験の課題で キレート滴定では 緩 Yahoo 知恵袋
薬品分析化学Ⅱ 講義 第2学年 前期 必修 15単位 《担当者名》准教授/村井 毅 概 要 「薬品分析化学Ⅰ」に引き続き、分析化学の基礎理論および容量分析法による医薬品の分析について学習する。滴定中に生じる液温変動は,実測値で2 ℃以内を許容しjis z 8703 試験場所の標準状態の温度1級を管理目標とした.jis r 3505 ガラス体積計の10誤差の試験方法に定める試験中の温度変化2 ℃/hを超えないに基づいた. 液温変動 湿度10 級 ±10 湿度 級 ± 湿度5 級 ± 5るキレート滴定の指示薬として,ph 10の緩衝溶液とあわ せて用いられている 11, 12)。ebtのキレート形成や,フェ ノールフタレインやメチルオレンジ溶液の包接化合物な ど,指示薬の呈色に共存する物質が影響を及ぼすことがあ ることは,心にとめておき




物理学実験及び同実験法 2 単位 生物学実験及び同 Manualzz



Column
(5) 滴定・終点操作 (ア) 手際よく滴定操作ができている。 (イ) 終点の判断が適切である。 3 完成度・結果について 1 報告書 (1) 反応式・計算式など必要なものが記入されている。 (2) 反応式に基づいた計算が正しくされている。 (3) 誤差を考慮している。報文 キレート滴定法による加硫ゴム中の亜鉛, カルシウム,マグネシウムの迅速定量 (昭和35年3月25日 受理) 田 下 森 藤 松 大 キ キ キ 文 雄夫弘 秀 要 旨 加硫ゴムを550℃ 以下の温度で灰化後,稀 塩酸にて溶解し不溶物は游別する沖 液を2n塩 酸酸性キレート試薬 技術的な内容に関するお問い合わせ先:カスタマーサービス部 free fax free dial 在庫や価格(記載容量以外もしくは特注品) に関するお問い合わせ先:マーケティング部 tel fax キット類 酸 化




キレート滴定 資料検索 資料 全ての資料 全ての種類 関連順 詳細リスト ハッピーキャンパス



Syllabus Kosen K Go Jp
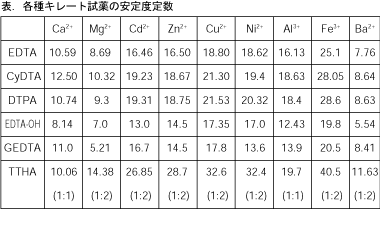
滴定の種類:キレート滴定(光度検出) 参考規格・文献 上水試験方法 硬度 総硬度 自動滴定装置 GT0 光度検出装置 GT-LDⅡ 干渉フィルター波長 6nm 滴定液 0.01mol/L-EDTA溶液 (試験研究用) 試薬 アンモニア緩衝液(pH10)・・・塩化アンモニウム67リウム滴定およびヨウ素滴定につ い て紹介する。 3.1 過マ ンガン酸力リウム滴定 過マ ンガン酸カリウムは強い 酸化剤 (eo=1,51 v)であ り,入手しやすく安価なため,広く用いられる 。 過マ ンガ ン酸カリウム滴定による過酸化水素水の濃度決定は代表的2 キレート効果および安定度定数 お待ちかねのキレート(Chelate)へ 話を 進めます語 原はギリシャ語 "Chele"でか にのハサミの意です文 頭のスケッチのよう に偶然,日 本の昔話の一場面とよく一致しま すねも う一つ,簡 単な実験を行なってみま



学生実験をみてみよう 第2期 その5 キレート滴定 江頭教授 東京工科大学 工学部 応用化学科 ブログ



Fukui C Ed Jp
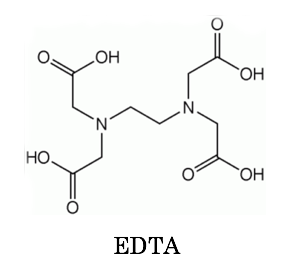
キレート滴定 1.目的 キレート滴定法を用いて、未知試料中に含まれる金属イオン(Ca 2+、Mg 2+)の濃度 を調べ、さらに水の硬度についても計算して求める。また、実験を通してキレート滴定法 の原理や操作の仕方について学び、結果の考察をしてさらに理解を深める。ChemicalsEvaluationandResearchInstitute,Japan ©16CERI,Japan 不確かさ評価におけるばらつきとは・・・ 4 ℃ ℃=195℃〜5℃の範囲キレート滴定に汎用されるキレート試薬;EDTA(六座配位子) ethylenediaminetetraacetic acid エチレンジアミン四酢酸 >NCH 2CH 2N< CH 2 COOH HOOCH C CH 2 COOH HOOCH C EDTAと金属との反応比は1:1 試薬としては 2Na塩を入手 M Y MY K MY = MY/MY キレート生成定数



キレート滴定の濃度計算問題についてです 解き方がわからないので 教えていただ Yahoo 知恵袋




Enjoy Learning プロジェクト 名城大学
キレート滴定(キレートてきてい、chelatometric titration )とは、錯滴定の一種で、錯形成試薬としてキレート試薬と呼ばれる多座配位子を用いるもの。 この容量分析法は金属 イオンの迅速で簡単な定量法の1つとして広く用いられている。 主なキレート試薬としてEDTA(エチレンジアミン四酢酸¦ 解明したことは 様 つぎのように 時 滴定したとき 毎 試料ごとに 訳 ~のわけではない ルール3 補助動詞は,平がなで表記する。 表2 平がな書きする補助動詞 漢字 用法 漢字 用法 漢字 用法 言 ~という意味である 見 計算してみる 出 動きだすキレート滴定 キレート滴定はキレート試薬が金属イオンと錯体 (キレート)を形成することを利用して金属イオン濃度を求める分析法である。 キレート試薬は金属イオンと結合して環状構造の錯体を形成する有機化合物であり、錯体はキレート環と呼ばれ



基礎から学ぶ分析化学 株式会社 化学同人



キレート滴定で水の中のカルシウムイオンの定量を調べる実験 Yahoo 知恵袋
考察のヒント あるいは小さすぎる 場合は誤差がおおき くなる。それはなぜ か?はどの程度で測 定するのが適当か? 考察のヒント ・電位差滴定では決定 できないのか? ワンポイント mol dm3をMと表記 する事もあるが正しく ない。
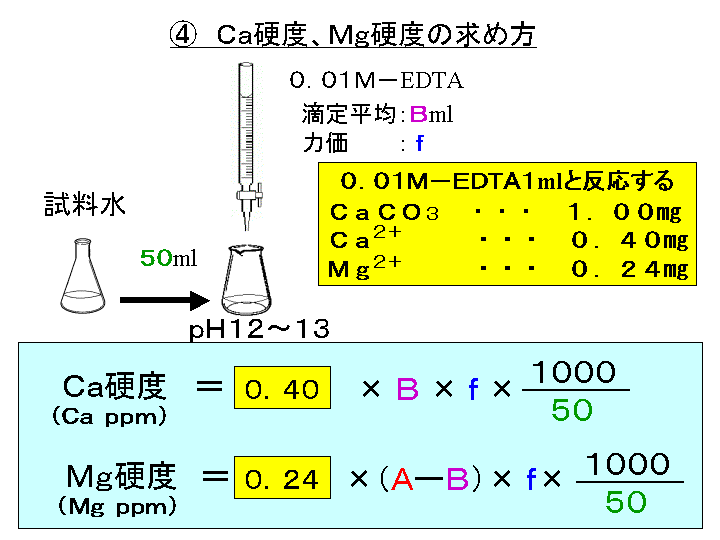



水の硬度測定 キレート滴定
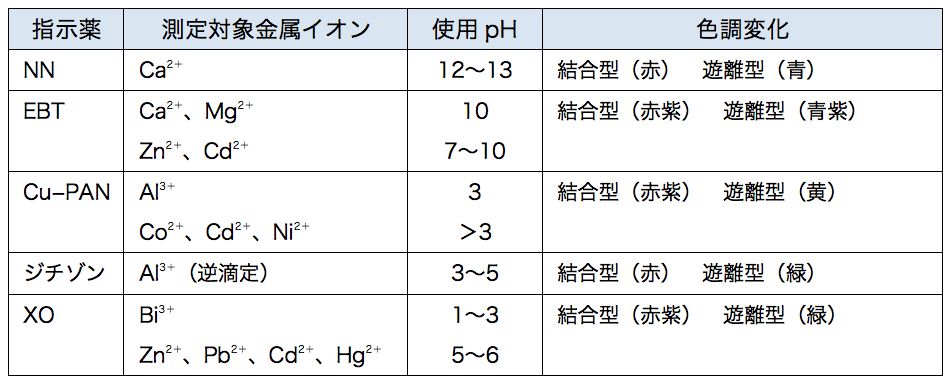



キレート滴定 Yakugaku Lab




ガロテクト モニターキャンペーン開催中です 22年1月31日 月 まで ニュース 試薬 富士フイルム和光純薬
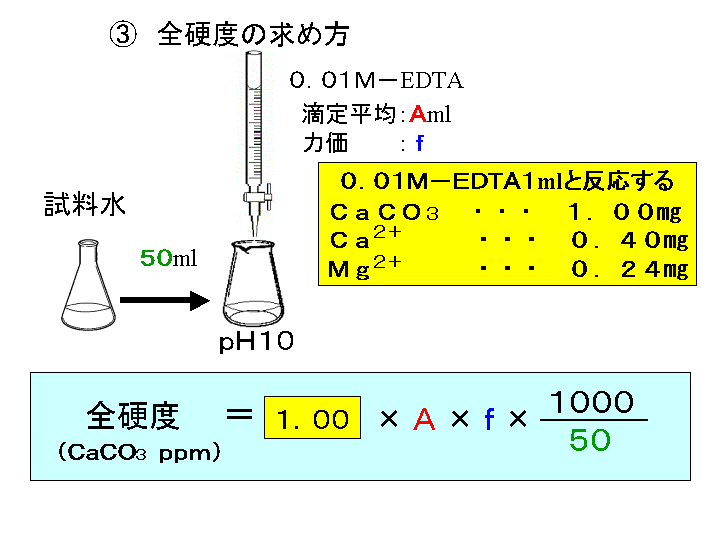



水の硬度測定 キレート滴定




Edta 分子か 双性イオンか Chem Station ケムステ



キレート滴定 Yakugaku Lab



Fukui C Ed Jp




第9回 食品の塩分の測定 硝酸銀滴定法 栄養士のための食品学実験



化学の中和滴定のレポートを作成しています 実験値の誤差 信頼 Yahoo 知恵袋




キレート滴定 資料検索 資料 全ての資料 全ての種類 関連順 詳細リスト ハッピーキャンパス



キレート滴定の実験でedta塩を精秤せず亜鉛を精秤したのですが Yahoo 知恵袋




京都大学 化学実験操作法 操作法 2 4 キレート滴定 Mg イオンの定量 Youtube




硬度1500mg Lのかた い水がある 水の硬度測定 バイオ科 応用バイオ化学実験 分析化学 2年 036 ブログ 学校のいまを知る 専門学校 東京テクニカルカレッジ




シラバス Manualzz



化学実験 キレート滴定 での考察の書き方が分かりません 実験で全硬 Yahoo 知恵袋




アドバンス講座 第2回 開催 実験の記録 サイエンスラボ 福井県教育総合研究所



Tsuruoka Nct Ac Jp




ミツロウラップ 蜜蝋 ラップ 天然素材 マイクロプラスチック ファイバー 洗濯ネット Sdgs エシカル 海洋汚染 Attitude サスティナブル 3枚セット 地球環境 L 脱プラ M 温暖化 プラスチックフリー 通販 S




アンモニア アミン類 配位結合 結合を形成する2つの原子の一方からのみ結合電子が分子軌道に提供される化学結合 Ppt Download



キレート わかりやすく



理工系 化学実験 株式会社 東京教学社




資料広場 オススメ資料 文書 最新資料 詳細リスト ハッピーキャンパス



夏休み21 高校生対象 群馬大学1日体験化学教室7 31 リセマム
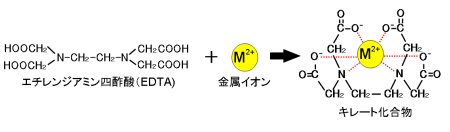



水の硬度測定 キレート滴定



水の硬度 株式会社ユニケミー ユニラボ
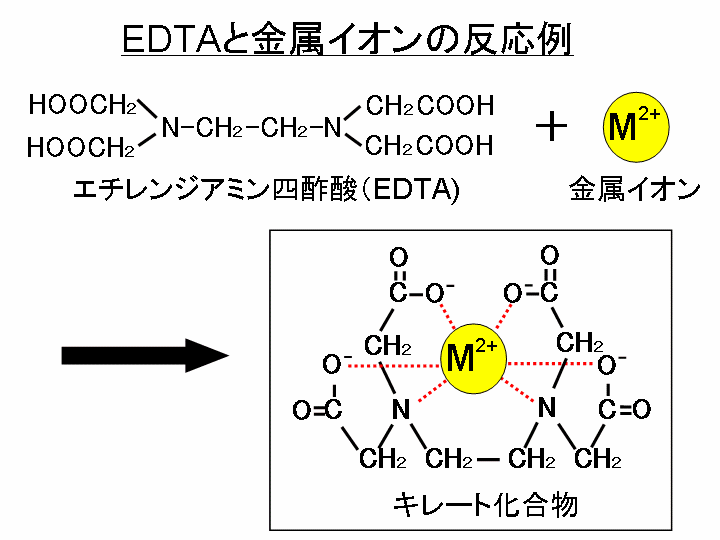



水の硬度測定 キレート滴定
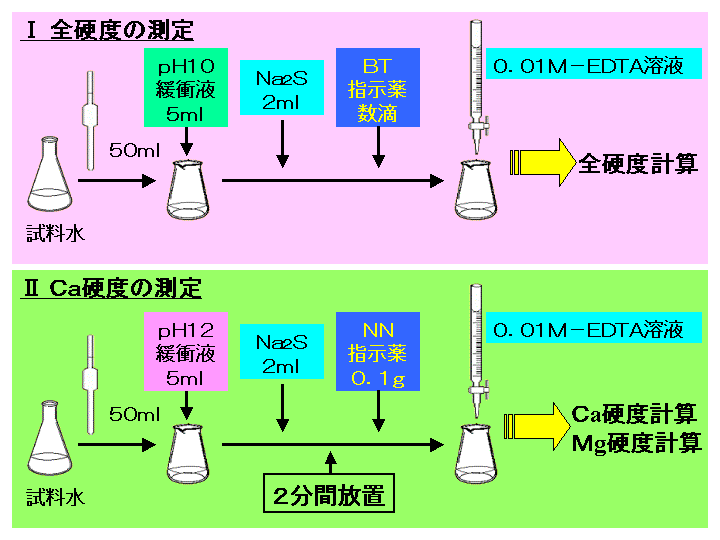



水の硬度測定 キレート滴定



Meijo U Ac Jp



Ous Repo Nii Ac Jp




分析化学 角田 欣一 渡辺 正 著 紀伊國屋書店ウェブストア オンライン書店 本 雑誌の通販 電子書籍ストア



上 キレート滴定 考察 キレート滴定 カルシウム 考察
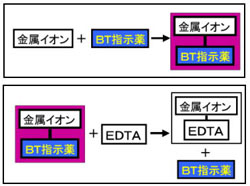



水の硬度測定 キレート滴定




キレート滴定 資料検索 資料 全ての資料 全ての種類 関連順 詳細リスト ハッピーキャンパス




土 日開講 分析化学応用学科 実験を繰り返して プロになる せんせのブログ 日本分析化学専門学校




キレート滴定 資料検索 資料 全ての資料 全ての種類 関連順 詳細リスト ハッピーキャンパス



キレート滴定 ちぇすなっちゅりー 獣医学生の日録



三重大学伊賀研究拠点実験実習 三重県立上野高等学校




キレート滴定 資料検索 資料 全ての資料 全ての種類 関連順 詳細リスト ハッピーキャンパス



キレート滴定で水の中のカルシウムイオンの定量を調べる実験 Yahoo 知恵袋



Fumi Theory Com




3 東京海洋大学 海洋科学部 Manualzz



Ricen Hokkaido C Ed Jp



逆滴定って何が逆なのですか たしかにそーだ どっちかっつーと 逆滴定 Yahoo 知恵袋




愛媛県立松山中央高校 19さが総文 みらいぶ 高校生サイト



Nagoya Repo Nii Ac Jp



Kuchem Kyoto U Ac Jp




55期生通信 D 選抜特進 アーカイブ



化学の中和滴定のレポートを作成しています 実験値の誤差 信頼 Yahoo 知恵袋



水の硬度 株式会社ユニケミー ユニラボ
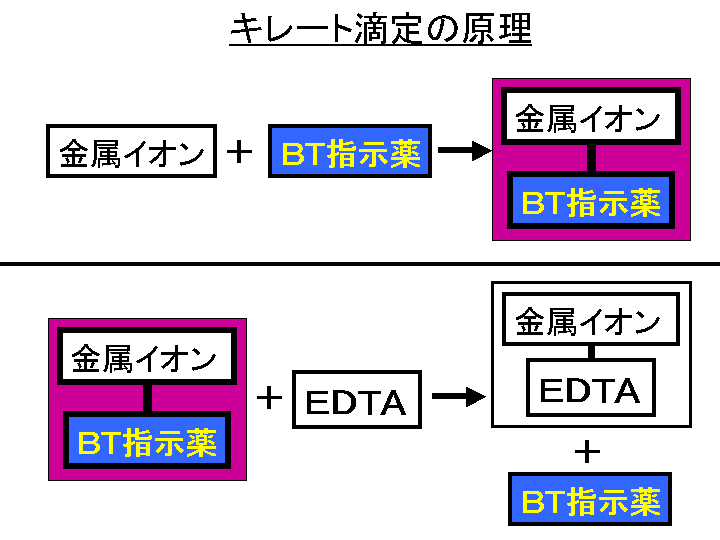



水の硬度測定 キレート滴定



食品学実験で無機質の定量 鉄の定量 をしました 結果は写真のように Yahoo 知恵袋




アドバンス講座 第2回 開催 実験の記録 サイエンスラボ 福井県教育総合研究所



キレート滴定で緩衝液を入れすぎるとどうなるんでしょうか N Yahoo 知恵袋




Edta 分子か 双性イオンか Chem Station ケムステ



Ricen Hokkaido C Ed Jp
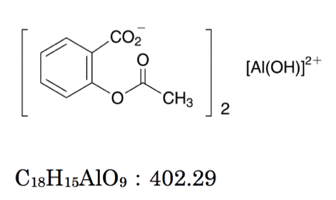



キレート滴定 Yakugaku Lab




硬度1500mg Lのかた い水がある 水の硬度測定 バイオ科 応用バイオ化学実験 分析化学 2年 036 ブログ 学校のいまを知る 専門学校 東京テクニカルカレッジ



基礎分析化学 株式会社 化学同人



キレート滴定の実験で Edtaの滴下量の誤差が0 2ml以内になるようにしな Yahoo 知恵袋



Nyuzen H Tym Ed Jp
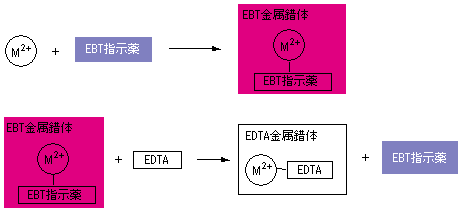



上 キレート滴定 考察 キレート滴定 カルシウム 考察



Gakusen Ac Jp




土 日開講 分析化学応用学科 水から鉱物の分析へ せんせのブログ 日本分析化学専門学校
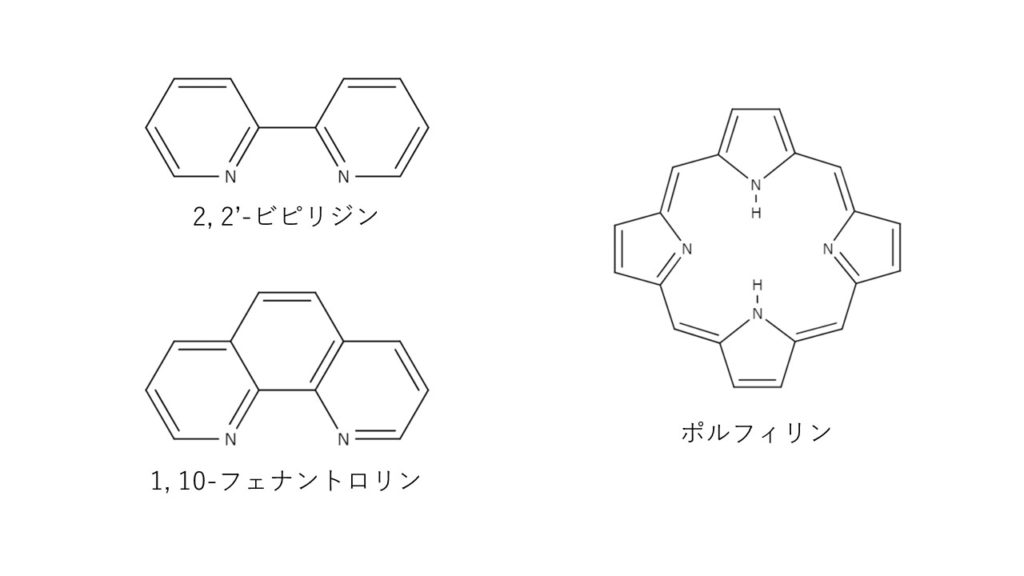



キレート滴定の原理とエチレンジアミン四酢酸 Edta の性質についてわかりやすく解説 ジグザグ科学 Com




水道水と飲料水の硬度測定 硬度 キレート滴定 マスキング剤 Transblog



Asahikawa Nct Ac Jp




水の硬度測定 キレート滴定



Chem Kyushu Univ Jp




キレート滴定




土 日開講 分析化学応用学科 水から鉱物の分析へ せんせのブログ 日本分析化学専門学校




キレート滴定 Yakugaku Lab



水の硬度測定 キレート滴定
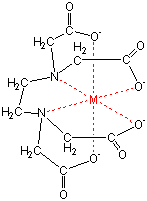



水の硬度測定




キレート滴定




誰でもできる 化学濃度計算 丸善出版 理工 医学 人文社会科学の専門書出版社



Dojindo Co Jp



三重大学伊賀研究拠点実験実習 三重県立上野高等学校



水の分析




キレート滴定




水道水と飲料水の硬度測定 硬度 キレート滴定 マスキング剤 Transblog
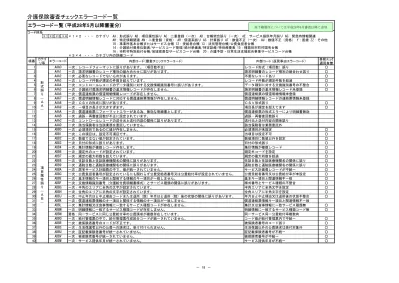



Microsoft Word 目次注意事項2 Doc



化学キレート滴定の問題です 赤線引いたところの意味がわかりません Yahoo 知恵袋




水の硬度測定 キレート滴定




キレート滴定 資料検索 資料 全ての資料 全ての種類 関連順 詳細リスト ハッピーキャンパス




キレート滴定 資料検索 資料 全ての資料 全ての種類 関連順 詳細リスト ハッピーキャンパス




硬度1500mg Lのかた い水がある 水の硬度測定 バイオ科 応用バイオ化学実験 分析化学 2年 036 ブログ 学校のいまを知る 専門学校 東京テクニカルカレッジ



至急 化学について質問です 実験の考察をしなくてはいけないのですが分か Yahoo 知恵袋



年11月発行 カルシウム塩のキレート滴定について




キレート滴定 資料検索 資料 全ての資料 全ての種類 関連順 詳細リスト ハッピーキャンパス



0 件のコメント:
コメントを投稿